水素は燃焼しても水しか生成しないクリーンなエネルギーとして、利用拡大が望まれています。しかし水素は、以下のような問題点を抱えています。まず、現在水素の主要な原料は天然ガスであり、水素を製造すると二酸化炭素も同時に発生するので、二酸化炭素削減につながらないということ[1]です。将来的には太陽電池や風力発電で作った電気を使って水を電気分解して製造した環境に優しい水素が主流になると期待されますが、現在はコスト面からそれは主流となっていません。そして極めて軽いガスであるために、乗り物の燃料にするにはかなり高圧(実用化されている燃料電池自動車は700気圧程度)にする必要があり安全面などで懸念があること、また高圧にしても単位体積当たりのエネルギーが少ないこと(ガソリンが35 MJ/Lであるのに対して水素は700気圧でも5MJ/L)などです。
これらの問題点に対処する一つの方策として、アルミニウムを使って水素を得る方法が考えられています。アルミニウムは両性元素であり、酸、アルカリいずれの水溶液とも反応して水素が発生します。また地球上の存在量が非常に多く、比較的安価でもあります。このことを利用して、例えば日本のあるベンチャー企業では、リサイクルされにくいアルミニウム資源(食品や薬品の包装材料など)からアルミニウム金属をとりだし、それとアルカリ水溶液を反応させて水素を得る方法を開発しています[2]。今回はごく最近発表された別のアプローチについてお話ししましょう。
さてガリウムは融点が30℃と低く、インジウムやスズとの合金とするとさらに融点が下がり室温でも液体となります。このようなガリウムの合金をアルミニウムに添加すると中性の水でもアルミニウムと反応して水素が発生することは10年以上前に報告されています[3]。この場合の主たる反応生成物は水素とベーマイトALOOHであり、後者は水処理などに活用できるとのことです(次反応式参照)。
Al + 2H2O → (3/2) H2 + AlOOH (1)
この方法でのアルミニウムの利点は単位体積当たりのエネルギーが大きいことで(86 MJ/L)、また他の金属よりもはるかに軽量であることです。しかしこの方法の最大の欠点は高価なガリウム合金を使うことで、これまでは使う度に新しいガリウム合金の添加が必要でした。反応後回収して再利用できれば実用化への大きな一歩を踏み出すことができます。
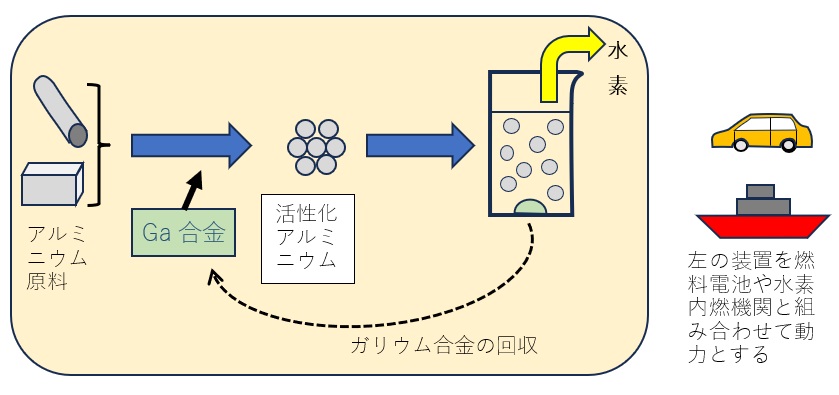 図1 アルミニウムを燃料として水素を得る過程の概念図
図1 アルミニウムを燃料として水素を得る過程の概念図
最近MIT(米国マサチューセッツ工科大学)の研究者らは、アルミニウムによる水素発生の反応条件や添加物を詳しく検討し、水素発生の反応後にガリウム合金を高効率で回収できる方法を見つけました[4]。彼らの方法(図1)ではまずアルミニウム粒にガリウム合金を加え、200℃に加熱し、その後冷却して48時間放置したものを使います。この処理によってアルミニウムの反応活性が極めて高まり、水とも素早く反応するようになります。(1)の反応によって、アルミニウムからほぼ理論通り水素を得ることができました。しかし、純粋な水(以下純水)との反応では、ガリウム合金も反応してしまい、それを回収することは不可能でした。しかし純水ではなく、食塩などの塩類を含む水と反応させると反応後ガリウム合金が容器の底にたまって回収できることが分かったのです。3M(3 mol/L)の塩化ナトリウム水溶液を使った場合は、100%の回収率でガリウム合金を回収できることが分かりました。水素も理論通りの量が発生しましたが、反応速度が純水の時と比べて1/300になってしまいました。0.6 Mの食塩水(海水とほぼ同じ濃度)の時も、ガリウム合金の回収率は100%でしたが、反応速度は純水の時の約1/100でした。食塩水中ではガリウム合金の微細な粒の回りに2重にイオンの層が生成し、それらが水との反応を妨げることでガリウム合金の回収ができたと彼らは推定しています。
さらに研究者たちは、ガリウム回収率は下げずに、水素発生の反応の速さを増すための触媒について検討しました。様々な物質を検討した結果、有機物のカフェインやイミダゾール(図2)が良い結果を与えることが分かりました。様々な濃度の組み合わせで実験を行い、最終的に食塩水の濃度が0.01 M、イミダゾールの濃度が0.02 Mの時、ガリウム合金回収率100%を保ったまま、反応速度は純水の時の2倍となることを見いだしました。
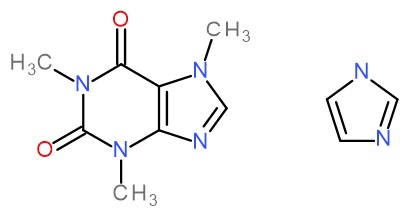 図2 カフェイン(左)とイミダゾール(右)の構造
図2 カフェイン(左)とイミダゾール(右)の構造
今回の研究からは、水素の代わりにアルミニウムをエネルギー源として自動車や船舶などに載せ、水素を発生させてエンジンの燃料に使うということが考えられます。水も必要ということから、論文では船舶や潜水艇への応用が現実的ではないかと指摘されています。ただ、本研究ではガリウム合金処理を行ったアルミニウムを1回の実験で約0.3g使うという条件で行っています。これを実用的なスケールに持って行くには多くの困難があると思われますが、新たな水素供給の道につながる重要な成果だと思います。水素社会に向けてまだまだこれからも様々な努力が続けて行かれることでしょう。それではまた次回。
[1] このブログの2021年4月ころの記事。https://www.kojundo.blog/news/4879/
[2] NEDO(新エネルギー・産業技術総合開発機構)のwebマガジン2022年8月。https://webmagazine.nedo.go.jp/practical-realization/articles/202204Alhytec/
[3] J.T. Ziebarth, J.M. Woodall, R. Kramer, G. Choi, Int J Hydrogen Energy 2011, 36:5271-9.
[4] A. Kombargi, E. Ellis, P. Godart and D. P. Hart, Cell Rep. Phys.-Sci. 2024, 5, 102121.
坪村太郎
最新記事 by 坪村太郎 (全て見る)
- 画期的なインフルエンザの検査方法となるか:味覚で感じる検査方法 - 2026年3月26日
- 炭素の新しい同素体:C48 - 2026年1月20日
- 2025年 ノーベル化学賞:3次元空間を自在にデザイン。空孔をもつ錯体化合物 - 2025年12月3日