
元素記号S、原子番号16の元素、硫黄。温泉地帯などで、黄色い結晶をみたことがあるだろうか。硫黄は天然に単体で産出される数少ない元素のひとつだ。日本の知床硫黄山では、1936年に大量に硫黄が噴出したことが記録されている。山頂付近で硫黄の結晶の塊が今でもたくさん見られる。火山の専門家によると、知床硫黄山の地下では溶融硫黄の蓄積が進行中の可能性が高いそうだ。また火山地帯では、単体の硫黄の他にも、毒性の高い硫化水素ガスや亜硫酸ガス(二酸化硫黄)が噴出していて、その濃度の測定が行われている。ある値を超えると市民や観光客に注意喚起や避難を促すようにしている。

左:知床硫黄山の山頂付近で見られる硫黄の結晶(写真提供ご協力:Viki Pandit氏)
右:実験室で得られる硫黄の結晶(写真提供ご協力:結晶美術館ホームページ管理者)
大気中の硫化水素の許容濃度(労働者が1日8時間、1週間40時間程度、有害物質に曝露される場合に、その数値以下であれば、健康上の悪い影響が見られないと判断される濃度)は5 ppmと設定されている。400 ppmを超えると生命に危険が生じ、700 ppmを超えると即死するとされている。
硫化水素はよく「卵が腐ったような臭いがする」と言われる。ゆで卵は他の調理法の卵に比べても臭い。これは硫黄を含むアミノ酸がゆでる際の熱で分解して、実際に硫化水素を発生するからだ。動物性のタンパク質、特に髪の毛には硫黄が多い。その理由は硫黄を含むメチオニンやシステインなどのアミノ酸が含まれているからだ。動物の毛を燃やすと臭いにおいが発生するのも含まれているその硫黄からくる。硫黄といえば、硫黄酸化物SOxが酸性雨の原因となるとして発生抑制が求められている。産地にもよるが、石炭や原油に含まれている硫黄成分が燃焼によってSOxとなることから大気汚染を起こさないためにも脱硫技術が不可欠となっている。
硫黄を含む「臭い」化合物にはいろいろと種類がある。都市ガスやプロパンガス、それら自身にはにおいがないが、可燃性であることから漏れによる事故を防ぐためにわざと“クサい”化合物が混ぜられている(付臭剤という)。付臭剤には、人体への毒性がないことや、危険を知らせるためにやや不快で、微量でも臭いが分かることが求められる。付臭ガスは、都市ガスなどにわずか2 ppm(体積換算で50万分の1)ほどが添加されているが、我々は十分にその臭いを認識することができる。
東京ガスでは、付臭剤として10年くらい前までは、「ターシャリーブチルメルカプタン(TBM):タマネギが腐ったような臭い」と「ジメチルサルファイド(DMS): ニンニクのような臭い」を混合したものを使用していたが、現在は、TBMと「シクロヘキセン(CH)を混合したものが利用されている。その理由は環境への配慮で燃やしたときにSOxをできるだけ出さないためである。その他、付臭剤としてはテトラヒドロチオフェンやエチルメルカプタン(エタンチオール)も使わる。エタンチオールは、ギネスブックにおいて世界一臭い物質として認定されている(2015年)。ちなみに人間が臭いを探知できる限界の濃度(閾値)は、エタンチオールで0.00007 ppm、TBMで0.000029 ppmであり、それらがいかに臭いかがその値からも推察できる。
実験1 消しゴムをつくってみよう~高分子の加硫実験~
加硫反応によって、天然ゴムの分子間に硫黄による架橋を作る(-C-S-C-)ことができる。加硫することにより天然ゴムの弾性・引張強度等の物理的性質が改善される。天然ゴム引っ張ると簡単に切れてしまうが架橋ゴムは簡単に切れることがなくなる。
準備する試薬:天然ゴム1 g、トルエン9 g、ケイ砂1 g、亜鉛華(酸化亜鉛)0.1 g、酸化チタン0.4 g、ジペンタメチレンチウラムテトラスルフィド(加硫剤)薬さじ1杯、ジブチルジチオカルバミン酸亜鉛(加硫促進剤)薬さじ1杯
1)天然ゴム1 g(板状など)をできるだけ小さく切ってガラスのビーカーに入れ、9 gのトルエンを加え、パラ フィルムなどでビーカーを覆い、トルエンが蒸発しないようにして一晩放置する。だんだんと天然ゴムがトルエンに溶けてゼリー状になる。
2)上のゼリー状になった溶液にケイ砂1 g、亜鉛華(酸化亜鉛)0.1 g、酸化チタン0.4 gを順に入れて、ガラス棒で均一になるまで攪拌する。
3)さらにそのビーカーに、ペンタメチレンチウラムテトラスルフィド(加硫剤)薬さじ1杯、そしてジブチルジチオカルバミン酸亜鉛(加硫促進剤)薬さじ1杯を順に入れてかきまぜる。それをドラフト内で120℃に熱したホットプレートにおいて約15分間ガラス棒で攪拌し続けると加硫反応が進行する。
4)ビーカーの中をシャーレに移し替えて、薬さじの平らな部分を利用して、糊のようなべたつきがなくなるまで、広げたりはがしたりしながら、同じホットプレート上で加熱を続ける。
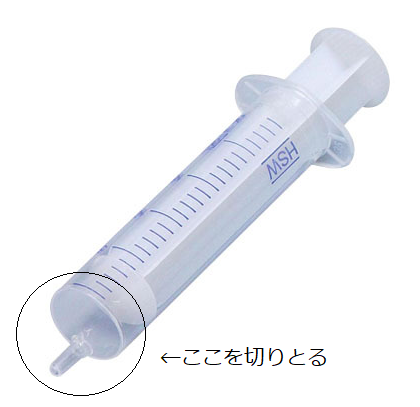
5)プラスチック製のディスポーザブルシリンジ(注射器)の先端を切ったものに、4)の加硫済みのゴムを入れ、押し出して円筒状に成型する。放置して乾燥すると消しゴムの出来上がり。
実験2 硫黄の相変化~17歳が指摘した教科書の間違い~
硫黄には同素体の種類は30種類といわれている。簡単な実験で単斜晶、斜方晶、ゴム状などの同素体を観察することができる。
1)斜方晶の硫黄
硫黄粉末1 gを乳鉢・乳棒でよく砕いてから、試験管に入れる。ここに二硫化炭素約5 mLを加えてから、試験管にコルク栓をしてよく振って溶かす。溶けない粒が残っていたらろ過して除去する。ろ液をシャーレまたは時計皿に移して、二硫化炭素が蒸発するのを待つと、斜方晶の硫黄が得られる。

斜方晶の硫黄(写真提供ご協力:結晶美術館ホームページ管理者)
2)単斜晶の硫黄
試験管の下半分ほどまで粉末硫黄を入れて、ガスバーナーの弱い炎でゆっくりと加熱すると、融解して液体になる。この液体を、ろ紙をセットしたガラスの三角漏斗に流して静置する。ろ紙に接した部分が固化してきたら、溶けた液体の硫黄分を別の入れ物に流しだして、すばやくろ紙を広げると、淡黄色の針状結晶を観察することができる。

単斜晶の硫黄(写真提供ご協力:結晶美術館ホームページ管理者)
3)ゴム状硫黄
試験管の下半分ほどまで粉末硫黄を入れて、ガスバーナーの弱い炎でゆっくりと加熱すると、融解して液体になる。さらに加熱を続けると液体が赤っぽい色に変わり、粘りが出てくる。まださらに加熱を続けると粘性が減って流動性がまた高くなる。これで加熱をとめて、水をはったビーカーに中の液体を流していくと、ゴム状のつながった硫黄を得ることができる。硫黄粉末の純度が高いほど、黄色に近い色となり、不純物が含まれていると茶褐色のゴム状硫黄となる。
ゴム状硫黄は、250℃まで硫黄を加熱するとできる。50万個以上の硫黄原子が繋がった直鎖状硫黄分子が形成されたものである。

ゴム状硫黄(写真提供ご協力:結晶美術館ホームページ管理者)
多くの高校化学の教科書で「ゴム状硫黄」の色は褐色と記されていた。2007年当時、鶴岡高専物質工学科3年生の高橋さん(17)が、実験的に純度が高い硫黄では黄色になることを確かめた。指導教員が出版社に訂正を申し入れ、教科書の修正につながった。
実験3 鉄と硫黄の化合~見ごたえがあるが事故も多い実験~
鉄粉3.5g、硫黄2.0gを乳鉢に入れて、乳棒でよく混ぜ合わせる。鉄と硫黄の質量比7:4はモル比を同じにするため。混ぜたものを試験管に入れ、試験管の上を脱脂綿でかるく蓋をする。ガスバーナー(ガスコンロでも可)で混合物の上部を加熱する。鉄と硫黄が化合する反応では、途中まで加熱し、火を消しても反応で発生した熱によって自発的に反応が進行する(動画参照)。
Fe + S → FeS

硫黄と鉄の反応の様子
写真・動画提供ご協力:都留文科大学教養学部学校教育学科 山田暢司先生
上記のようなシンプルな化学反応が起こったことを目で見て確認するだけでなく、反応前には磁石に鉄が応答するが、反応後は磁石に応答しなくなること、また硫化鉄の生成を、試験管に希塩酸(2%程度で十分)を加えて硫化水素H2Sの発生をそのにおいから確認できる。
FeS + 2HCl → FeCl2 + H2S
【注意点】
※硫黄と鉄粉の混合が十分でない場合、硫黄の燃焼によって二酸化硫黄が発生することがある。二酸化硫黄は呼吸器を刺激するなどの毒性があるため、最初の混合を丁寧に行うこと。またドラフトの中で実験を行うか、十分な換気のもと実験を行う。
※硫化鉄の生成を確認するために、塩酸を試験管に入れて硫化水素の発生をそのにおいから確かめられる。硫化水素は有毒なので大量に発生させないために、使用する塩酸の濃度が十分に薄いこと(2%程度)。発生したガスを直接匂うのではなく、手で仰いで大きく吸い込まないように注意する。
参考文献:
桜井弘、「元素111の新知識(ブルーバックス)」、講談社、1997年
Viki Pandit氏のホームページ:https://www.vikipandit.com/the-fuming-iozan/
結晶美術館、硫黄のページ:https://sites.google.com/site/fluordoublet/elements/sulfur
池貝隆宏ら、「箱根山大涌谷の火山ガス濃度の推移」、神奈川県環境科学センター研究報告 No.40 (2017)
日本薬学会 環境・衛生部会、環境・衛生薬学トピックス「硫化水素は毒か薬か?表裏一体の性質」:http://bukai.pharm.or.jp/bukai_kanei/topics/topics53.html
公益社団法人におい・かおり環境協会、技術資料・嗅覚閾値のページ:
https://orea.or.jp/about/ThresholdsTable.html
川口健男・井田 誠夫、「消しゴムをつくる : 天然ゴムの加硫(<特集>身近なものをつくる化学実験)」、化学と教育42 巻 4 号 p. 258-259(1994)
武田一美・茂串圭男、「硫黄の実験」、化学と教育44 巻 4 号 p. 235-237(1996)
朝日新聞社:朝日新聞縮刷版平成21年1月号、朝日新聞出版、通巻 1051 号、p.254(2009)
らくらく理科教室、鉄と硫黄の化合:http://sciyoji.site/sciyoji/rk2_c_fe_s_sasa/
山﨑 友紀
最新記事 by 山﨑 友紀 (全て見る)
- 実験講座 番外編 アメリカ、サンフランシスコ湾での天然塩づくり - 2024年3月25日
- 実験講座 番外編 アメリカ カリフォルニアで見た多様な鳥たち - 2024年1月29日
- 実験講座 番外編 アメリカCalifornia Academy of Science(科学博物館)訪問 - 2023年11月27日