元素記号Se、原子番号34の元素、セレン。先に発見されたテルル(地球にちなんで名づけられた元素)の陰に隠れていた未知の元素であったことから、月(ギリシャ語Selene)にちなんでSelenium(英語)またはSelen(独語)の名前がつけられた。
セレンは酸素族に属する半金属の元素。ヒトには、毒性を示すが逆に必須の元素でもあるため、欠乏症も過剰症も発生しやすい元素のひとつである。生体内でセレンは酵素などのタンパク質を構成するのに使われ、抗酸化反応や甲状腺ホルモンの活性化と代謝に関係するなどの重要な役割を担っている。セレンは魚介類、肉類、海藻などに含まれているため、通常の食事をしていれば不足することはない。平均的に大人のヒトの体内に体重1 kg当たり約250 μgのセレンが存在する。
セレンの需要は幅広く、特異的な半金属の性質と電気化学的性質から、化合物半導体太陽電池(CIGS系)や医療用X線画像診断装置の主要材料として、また触媒や複写機(感光体部分)、顔料(赤)として用いられる他、医薬的にふけ防止シャンプーや抗癌剤としても利用されている。日本はセレンの世界第1位の生産国であり、2016年時点で年間約752トンが生産されている。

六方晶系の金属セレン(左)とその同素体の赤色で単斜晶系の金属セレン(右)
W. Oelenによる”Black, glassy amorphous (with thin layer of grey selenium) and red amorphous selenium” CC BY-SA 3.0(WIKIMEDIA COMMONS)
セレンはガラスの中で赤色やブロンズ色に発色する。また、ガラスの他の不純物の色を吸収してガラスを透明に見せることもでき、ガラス工業や陶磁器の着色に広く使われている。写真の赤い切子グラスはセレンが用いられたもので、銅による赤発色に比べて鮮やかな赤色を出すことができる。

セレンによる赤色発色させた切子グラス
写真提供:和ガラス専科ホームページ管理人 橋本勝彦氏http://wagarasu.sakura.ne.jp/index02.html
また、セレン化亜鉛ZnSeは、600 nm ~16 μmの領域の光(可視光線、赤外線、遠赤外線)おいて他の材料に比べると透過性が優れている。セレン化亜鉛はそれ自身による熱の吸収が少なく、熱衝撃にも強いなどの特徴を有するので、CO2レーザーなど、赤外レーザー用の透過材料や、すばる望遠鏡など大型天文台における赤外線観測用レンズに利用されている。写真はTAOプロジェクトで採用されている望遠鏡用レンズ。セレン化亜鉛のレンズの利用は活発に星生成を行っている遠方の銀河の分光観測を可能にしている。セレン化亜鉛はそれ自身による熱の吸収が少なく、熱衝撃にも強いなどの特徴を有するので、CO2レーザーなど、赤外レーザー用の透過材料や、すばる望遠鏡など大型天文台における赤外線カメラのレンズに利用されている。写真は東京大学アタカマ天文台(TAO)6.5m望遠鏡の赤外線カメラで採用されているセレン化亜鉛のレンズ。これによって高感度の赤外線観測が実現され、例えば遠方の星形銀河の分光観測などが可能となる。(2019年10月4日 改訂)
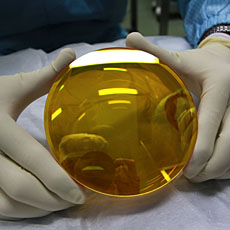
6.5 mTAO望遠鏡観測用のセレン化亜鉛レンズ
写真提供:東京大学TAOプロジェクトhttp://www.ioa.s.u-tokyo.ac.jp/TAO/news/20110531/index.html
実験1 SeO2による有機化合物の酸化反応
セレンSeは周期表で酸素族(第16族)の真ん中に位置する。酸素Oは3.44と強い電気陰性度を示すが、セレンSeは2.55と小さい値を示す。また酸素と炭素とは安定な二重結合を作るが、セレンは炭素と安定な二重結合を作らない。酸素と似ているようで異なる特性からセレンは、有機合成反応に利用されている。例えば二酸化セレンSeO2は有機化合物の酸化剤として活用されている化合物である。例えば下図のようにアリル位のCHを酸化して、アリルアルコールを与えることができる。他の合成方法では困難な酸化プロセスなので酸化セレンが重宝される。セレン化合物は有毒なのでその取扱いには注意し、ドラフト中で実験することが望ましい。
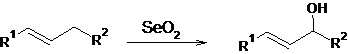
また、SeO2とケトンとを過酸化水素の存在下で反応させると次の反応式のように、アルキル基またはアリール基の転移を伴う酸化反応が生じるが、同じ酸素族の硫黄の酸化物SO2を用いても、同様の反応は起こらない。
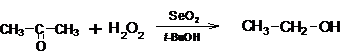
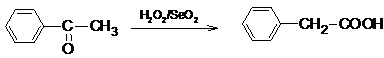
実験2 セレン汚染水の高度処理とその分析方法
セレンは自然界において-2価、0価、2価、4価、6価の5種類の酸化形態をもつ。汚染物質としては6価のセレン酸イオン(HSeO4―、SeO42―)または4価の亜セレン酸イオン(HSeO3―、SeO32―)の形態で存在する。我が国では法規制されていない時代に、顔料工場などから6価や4価のセレンイオンが排出されたため、土壌や水質が汚染された。やっかいなことに6価および4価のセレンは、ともに難溶性塩を生成しにくく容易に除去することができない。現在のセレン処理技術としては、イオン交換法、膜分離法、水酸化鉄Fe(OH)2による共沈、鉄(たとえばグリーンラスト*)による還元法などがある。
セレン浄化剤のグリーンラスト(Green Rust)は自然界にも存在する鉄の腐食生成物である。例えば化学式([Fe2+4Fe3+2(HO−)12]2+ • [SO2−4•3H2O]2−)で示され、強い還元力を有する層状構造から、特有のアニオン吸着能力を示す。
微量のセレンの定量分析には精密な分析技術が必要である。平成15年5月水道水質基準に関する改正がなされ、現在はICP発光分析法によって定量されているが、他の元素に比べてセレンはヒ素と同様にICPの測定感度が低く、複数の酸化形態を持つため、そのままでは正確に測定できない。ICP装置に導入する前にセレンのすべての酸化状態のものをまずは濃硝酸で6価(SeO42―)の状態に酸化する。そのあとに塩酸により還元して水素化しやすい4価(SeO32―)にし、水素化物(気体)のSeH2にして濃縮する。これらの前処理によって数ppbまたは検出限界50 ppt レベルの測定が可能となる。水素化にはICP付帯設備の水素化物発生装置を用い、水素化剤としては水素化ホウ素ナトリウムが用いられる。
参考文献:
国立健康・栄養研究所 「健康食品」の安全性・有効性情報https://hfnet.nibiohn.go.jp/contents/detail682.html
和ガラス専科~第2章ホームページ:
http://wagarasu.sakura.ne.jp/index02.html
洲脇康史・岡崎正規、「セレンによる土壞汚染と修復」、日本土壌肥料学雑誌第76巻第4号(2005)p.515-521
世界のセレン生産量 国別ランキング・推移:
https://www.globalnote.jp/post-3161.html
園田昇、「二酸化セレンによる有機化合物の酸化―オレフィンおよびアセチレン類の新しい酸化法―」、有機合成化学、第30巻第8号、p.739-745(1972)
林浩志、「グリーンラスト/フェライト循環処理法による セレン汚染水の高度処理」、資源と素材、Vol. 122, No.3, p.134-129 (2006)
東京大学アタカマ天文台 (TAO) 計画:
https://www.chem-station.com/odos/2009/07/-oxidation-with-seo2.html
日本天文学会欧文研究報告「すばる望遠鏡特集号」各論文の概要:
https://www.subarutelescope.org/Pressrelease/2011/04/07/j_index.html
山﨑 友紀
最新記事 by 山﨑 友紀 (全て見る)
- 実験講座 番外編 アメリカ、サンフランシスコ湾での天然塩づくり - 2024年3月25日
- 実験講座 番外編 アメリカ カリフォルニアで見た多様な鳥たち - 2024年1月29日
- 実験講座 番外編 アメリカCalifornia Academy of Science(科学博物館)訪問 - 2023年11月27日