


本年度のノーベル化学賞受賞者
左からKarl B. Sharpless(米国1941-), Morten P. Meldel(デンマーク1954-), Carolyn Bertozzi(米国1966-)
写真はWikipedia英語版より、https://en.wikipedia.org/wiki/Karl_Barry_Sharpless CC BY-SA 4.0、https://en.wikipedia.org/wiki/Morten_P._Meldal CC BY-SA 4.0、https://en.wikipedia.org/wiki/Carolyn_Bertozzi CC BY-SA 3.0
2022年度のノーベル化学賞は写真の3氏が受賞することとなりました。「クリックケミストリー」と「生体直交化学」の開発に対しての受賞となります。これらの意味は後で説明するとして、Sharpless 先生は2001年に日本の野依良治先生と米国のKnowles先生とともにノーベル化学賞を受賞されていて、なんと2回目の受賞となります。今回は主にノーベル財団の一般向けの説明[1]ともっと詳しい説明[2]をもとにその内容をご説明したいと思います。
 図1 クリックケミストリーのイメージ 誰でも簡単に2つの部品をつなげられる
図1 クリックケミストリーのイメージ 誰でも簡単に2つの部品をつなげられる
この数十年で有機化学は非常な発展を遂げ、どのような分子でも合成できるという時代となってきました。そうはいっても、様々な構造の分子を作るにはそれぞれの分子の構造に合わせた精密な合成指針が必要です。技術的に非常に難しい合成能力が必要な場合も多々あります。Sharpless先生は、様々な部品を用意して、それを簡単な道具で組み立てることができれば、一連の多くの分子を作ることができると考えました。「一連のブロック分子をつなぐことで小さな分子から大きな系まで作ることができる化学」をクリックケミストリーと名付けたのです。最近よく見られるベルトの樹脂製のバックルのようにだれでも「カチャッと」くっつけられるという化学反応を目指しました。参考文献[2]によれば、IKEAのFlatpack(家具のIKEAの組み立て家具のように部品がパッケージされていて誰でも簡単な工具さえあれば組み立てられる)のようなイメージとのことです。1990年代にはコンビナトリアルケミストリーという考え方が広まってきており、これは「機能に応じて狙った化合物を作る」のではなく、「絨毯爆撃的に多数の一連の物質を作り、その中から必要な機能を持ったものを探し出す」という考え方ですが、そのためにも一連の多数の化合物を簡単に合成できることが必要とされていたのです。
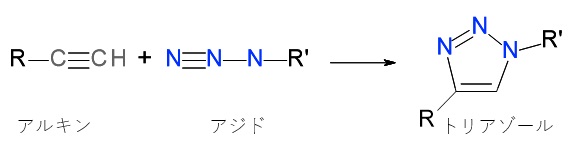
図2 アルキン(炭素原子間に三重結合をもった分子)とアジド(3つの窒素を持つ化合物)の反応でトリアゾールが合成できる。通常クリック反応というとこのタイプの反応をさす。
Sharpless先生らは、多くの化学反応を精査し、図2に示す反応,すなわちアルキンとアジドの反応が彼らの思うクリックケミストリーに使えると考えました。この反応はもとはといえば1960年にドイツのフーズゲン(Rolf Huisgen、1920-2020)が開発した反応です。しかし、高温でないと反応がなかなか進行せず、かつアジド類は爆発の可能性のある危険な化合物であり、この反応の利用は困難でした。ところが、2001年にMeldel先生らは銅化合物を触媒とすると低温でも速やかにこの反応が進むことを見出しました。ほぼ同時期にSharpless先生のグループも同じことを見つけていたのです。銅の1価の化合物が触媒として非常に効率よく働くこと、そして様々な置換基(図2におけるRやR’)をつけた場合でもスムーズに、しかも室温で反応が進むことが確認され、クリックケミストリーが世に出ることになりました。
さらにこれを生物学に研究に応用することも考えられていきました。Bertozzi先生は、生物における糖鎖(ぶどう糖などの糖分子が結合したもの)の重要性を研究されていました。例えば、細胞にはまわりに糖鎖が飛び出ている部分があり、それが重要な働きをしているのです。もし糖鎖の部分に例えば蛍光を出す分子を結合させることができれば、細胞のどこに問題の糖鎖があるかが分かります。何せ研究対象は生きた細胞なので、細胞の通常の営みを邪魔しないような化学反応を使う必要があります。先のクリックケミストリーで使われる反応は欲しいものを結合させることができるという点では良かったのですが、生物にとって毒である銅化合物を使うことが問題でした。そこでBertozzi先生は様々な反応を調べ、環状構造のアルキンを用いると触媒を使わずともクリック反応が進行することを見出したのです。この反応を利用して、細胞上の糖鎖の場所を調べる(マッピング)することに成功しました(この仕組みは図3に示しました)。この反応は生物内で起こっている反応を全く邪魔せず進行するという意味で生体直交化学と名付けられたのです[3]。
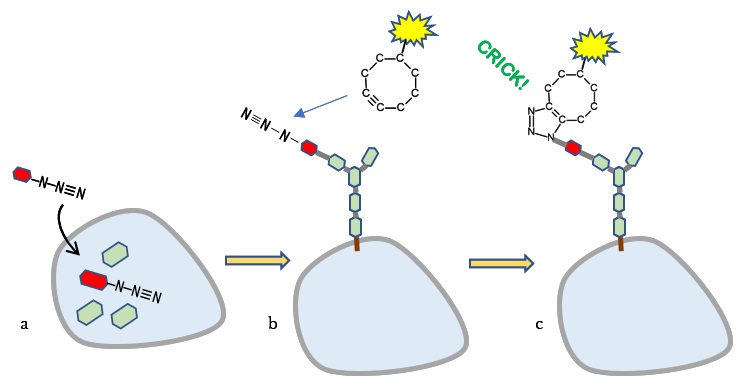 図3 a)細胞の中にアジド(-N-N≡N)が結合した糖分子を入れる。b)アジド化した糖を用いて細胞内で合成された糖鎖を細胞外に突き出す。c)細胞外でアジドと環状アルキン(蛍光を出す分子が結合されている)がクリック反応を行い、糖鎖の部分に蛍光分子が結合していることから、その蛍光を調べることで、糖鎖部分がどこにあるのかを知ることができる。
図3 a)細胞の中にアジド(-N-N≡N)が結合した糖分子を入れる。b)アジド化した糖を用いて細胞内で合成された糖鎖を細胞外に突き出す。c)細胞外でアジドと環状アルキン(蛍光を出す分子が結合されている)がクリック反応を行い、糖鎖の部分に蛍光分子が結合していることから、その蛍光を調べることで、糖鎖部分がどこにあるのかを知ることができる。
こうしてSharpless先生の夢から始まったクリックケミストリーは生物研究への応用まで実を結び、ノーベル賞受賞となったのです。先生方の独創性は素晴らしいですね。このような汎用性があり、かつ簡単に進行する反応がさらに見つかればもっともっと応用の可能性も広がると思います。それではまた次回。
[1] “Their functional chemistry works wonders”, https://www.nobelprize.org/uploads/2022/10/popular-chemistryprize2022-2.pdf
[2] “Click chemistry and bioorthogonal chemistry”, https://www.nobelprize.org/uploads/2022/10/advanced-chemistryprize2022-2.pdf
[3] グラフのxとy座標軸のように直交していると全く独立で両者を考えることができます。このような観点で複数の事象が独立に(互いに干渉せずに)ふるまう場合に、直交しているというようになったと考えられます。
坪村太郎
最新記事 by 坪村太郎 (全て見る)
- 画期的なインフルエンザの検査方法となるか:味覚で感じる検査方法 - 2026年3月26日
- 炭素の新しい同素体:C48 - 2026年1月20日
- 2025年 ノーベル化学賞:3次元空間を自在にデザイン。空孔をもつ錯体化合物 - 2025年12月3日